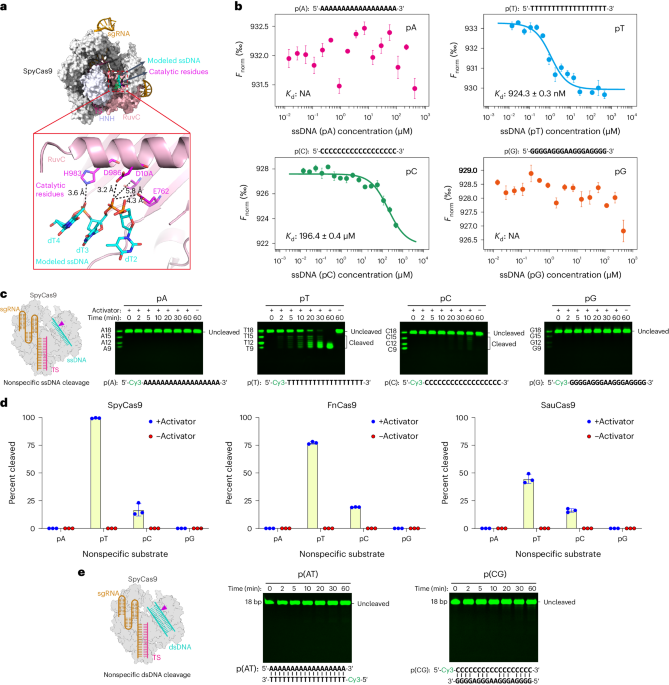
DNA 或 RNA 靶标结合激活 Cas9 的核酸转运酶活性
Makarova, KS, Zhang, F. 和 Koonin, EV SnapShot:2 类 CRISPR–Cas 系统。 细胞 168,328–328.e1(2017)。 文章 中科院 PubMed 谷歌学术 Cong, L. 等人利用 CRISPR/Cas 系统进行多重基因组工程。 科学 339,819–823 (2013)。 文章 中科院 PubMed PubMed Central 谷歌学术 Li, JF 等人。多重和同源重组介导的基因组编辑 拟南芥 和 本氏烟 使用引导RNA和Cas9。 天然生物技术。 31,688–691 (2013)。 文章 中科院 PubMed PubMed Central 谷歌学术 Nekrasov, V., Staskawicz, B., Weigel, D., Jones, JD […]
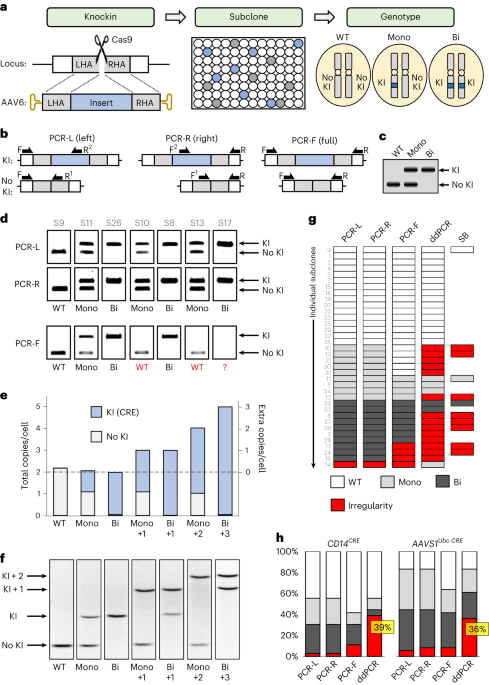
使用 Cas9 和 AAV 修复模板进行基因组工程可产生病毒载体的频繁串联插入
Vaidyanathan, S.、McCarra, M. 和 Desai, TJ 肺干细胞和囊性纤维化治疗。 在 肺干细胞在发育、健康和疾病中的作用 (Nikolić,MZ 和 Hoganheffield,BLM 编辑)306-321(欧洲呼吸学会,2021 年)。 伊藤,M.等人。 使用 CRISPR/Cas9 对源自隐性营养不良性大疱性表皮松解症 (RDEB) 的诱导多能干细胞 (iPSC) 进行无足迹基因突变校正 小猪巴克 转座子系统。 J.德马托尔。 科学。 98,163–172(2020)。 文章 中科院 考研 谷歌学术 威尔金森,AC 等人。 自体 HSC 中 β-珠蛋白的 Cas9-AAV6 基因校正可改善小鼠镰状细胞病红细胞生成。 纳特。 常见的。 12,686(2021)。 文章 中科院 考研 考研中心 谷歌学术 Khalil, AM 基因组编辑革命。 J.热内特. 工程师。 生物技术。 18,68(2020)。 文章 […]
通过多尾结构提高 mRNA 活性和寿命
由于信使 RNA (mRNA) 在多种 COVID-19 疫苗中的基石作用,信使 RNA (mRNA) 在大流行期间一跃成为公众关注的焦点。 但 mRNA(指导人体产生蛋白质的基因序列)也正在被开发为一类新型药物。 然而,为了使 mRNA 具有广泛的治疗用途,这些分子需要比构成新冠疫苗的分子在体内的持续时间更长。 来自麻省理工学院和哈佛大学布罗德研究所以及麻省理工学院的研究人员通过在分子中添加多个“尾巴”设计了一种新的 mRNA 结构,可将细胞中的 mRNA 活性水平提高 5 至 20 倍。 研究小组还表明,与未修饰的 mRNA 相比,他们的多尾 mRNA 在动物体内的持续时间延长了 2 至 3 倍,并且当纳入 CRISPR 基因编辑系统时,可以在小鼠体内实现更有效的基因编辑。 新的 mRNA,报道于 自然生物科技,有可能用于治疗需要长期治疗的疾病,这些治疗需要编辑基因或替换有缺陷的蛋白质。 mRNA 在新冠病毒疫苗中的应用非常棒,这促使我们探索如何扩展 mRNA 可能的治疗应用。 我们已经证明,非自然结构的功能比自然存在的结构要好得多。 这项研究让我们对化学和拓扑修饰 mRNA 分子的能力充满信心。” 新论文的资深作者、布罗德研究所核心成员、麻省理工学院化学助理教授王晓 “最令我兴奋的是,这种新形状的 mRNA 能够很好地被细胞翻译机制所耐受,”该论文的第一作者、麻省理工学院化学系王教授实验室的研究生 Hongyu Chen 说。 “这为合成修饰 mRNA 以扩展其治疗用途开辟了许多新的机会。” […]
新型“GPS纳米颗粒”对与肿瘤扩散有关的蛋白质提供基因冲击
宾夕法尼亚州立大学的研究人员表示,一种新开发的静脉注射“GPS纳米颗粒”可以瞄准癌细胞,向与肿瘤生长和扩散有关的蛋白质提供基因冲击。 他们在人类细胞系和小鼠中测试了他们的方法,以有效地敲除致癌基因,报告称该技术可能为众所周知的难以治疗的基底样乳腺癌提供更精确和有效的治疗。 他们今天(3 月 11 日)在 ACS纳米。 他们还提交了临时申请,为本研究中描述的技术申请专利。 我们开发了一种 GPS 纳米粒子,可以找到需要的位置。 一旦到达-; 并且只有那里-; 它可以传递基因编辑蛋白以防止癌细胞扩散。 这是一项艰巨的任务,但我们证明该系统适用于基底细胞样乳腺癌。” Dipanjan Pan,通讯作者,宾夕法尼亚州立大学纳米医学 Dorothy Foehr Huck & J. Lloyd Huck 讲座教授、核工程和材料科学与工程教授 与三阴性乳腺癌类似,基底样乳腺癌的发病率可能低于其他乳腺癌,但治疗起来却更具挑战性,主要是因为它们缺乏其他乳腺癌中发现的三个治疗靶点。 它们也往往具有攻击性,肿瘤生长迅速,脱落的细胞扩散到身体其他部位。 这些细胞可以种植更多的肿瘤,这一过程称为转移。 “转移是一个巨大的挑战,特别是对于三阴性乳腺癌和基底样乳腺癌等癌症,”潘说。 “这种癌症很难被发现,并且在常规乳房 X 光检查中不会显现出来,它主要影响可能尚未接受预防性护理的年轻人或非裔美国人。结果可能非常非常糟糕,因此有一个明确的证据:当癌症没有及早发现时,对更有效治疗的临床需求就得不到满足。” 该团队制造了一种特洛伊木马纳米颗粒,用专门设计的脂肪分子(看起来像天然存在的脂质)对其进行伪装,并将其装满 CRISPR-Cas9 分子。 这些分子可以靶向细胞的遗传物质,识别特定基因并将其敲除,或使其失效。 在这种情况下,该系统针对人类叉头框 c1 (FOXC1),该蛋白参与引发转移。 潘将设计的脂质描述为“两性离子”,这意味着它们在纳米粒子的外壳上具有接近中性的电荷。 这可以防止人体的免疫系统攻击纳米颗粒 -; 因为它伪装成一种无威胁的正常分子——; 并且可以帮助释放有效负载,但前提是脂质识别出癌细胞的低 pH 环境。 为了确保脂质仅在较低的 pH 值下激活,研究人员设计了它们,一旦进入酸性更强的肿瘤微环境,它们的电荷就会转变为正电荷,从而触发有效负载的释放。 但人体空间很大,那么研究人员如何确保 CRISPR-Cas9 有效负载到达正确的目标呢? 为了确保纳米颗粒能够与正确的细胞结合,他们附着了上皮细胞粘附分子(EpCAM),已知该分子可以附着在基底样乳腺癌细胞上。 潘说:“没有人尝试过利用环境响应传递系统来靶向基底样乳腺癌细胞,该系统可以从基因上敲除感兴趣的基因。” “我们是第一个证明这是可以做到的。” […]
CRISPR 传递的突破有望实现更安全的基因编辑
在该杂志最近发表的一篇评论中 美国国家科学院院刊研究人员探索非病毒和细胞特异性成簇规则间隔短回文重复序列 (CRISPR)-CRISPR 相关蛋白 (Cas) 递送方法,并强调其在研究和基因治疗应用中的优势。 学习: 体内基因组编辑器的靶向非病毒递送。 图片来源:Catalin Rusnac / Shutterstock.com 改善 CRISPR-Cas 酶的递送 CRISPR-Cas 酶可实现基因组编辑的精确性和简便性; 然而,它们也与某些安全问题有关,因为它们有可能引起永久性改变。 Cas9 特异性的增强标志着进步,但有针对性的递送对于最大限度地降低风险仍然至关重要。 病毒载体作为这些酶的递送载体已被广泛研究。 然而,这些系统也与免疫原性和遗传破坏的风险有关。 CRISPR-Cas 核糖核蛋白 (RNP) 和信使核糖核酸 (mRNA) 编码的核酸酶等新兴替代品可减少脱靶效应和肿瘤发生风险,但缺乏特异性靶向。 例如,Cas9 RNP 可提供短暂的细胞存在和成本效益,减少脱靶效应和免疫原性; 然而,他们的目标交付提出了重大挑战。 因此,仍然迫切需要先进的交付策略。 进一步的研究对于开发更安全、更精确的 CRISPR-Cas 系统传递机制至关重要,这将确保靶向基因组编辑具有最小的脱靶效应并降低临床风险。 离体 有针对性的交付方法 可以通过细胞的物理隔离来实现靶向递送 离体 基因组编辑。 这种方法对于造血细胞特别有效,可以在体外轻松分离和编辑造血细胞。 电穿孔等技术促进了 T 细胞以及造血干细胞和祖细胞 (HSPC) 的高效基因组编辑,从而为镰状细胞病 (SCD) 和 β 地中海贫血等血液疾病的治疗带来了独特的革命性潜力。 尽管其 功效电穿孔的一个重要限制是其对其他组织的适用性有限以及潜在的细胞毒性作用。 离体 基因组编辑也促进了再生医学的发展。 […]
