Hedgehog 通路抑制剂可改善 IPF
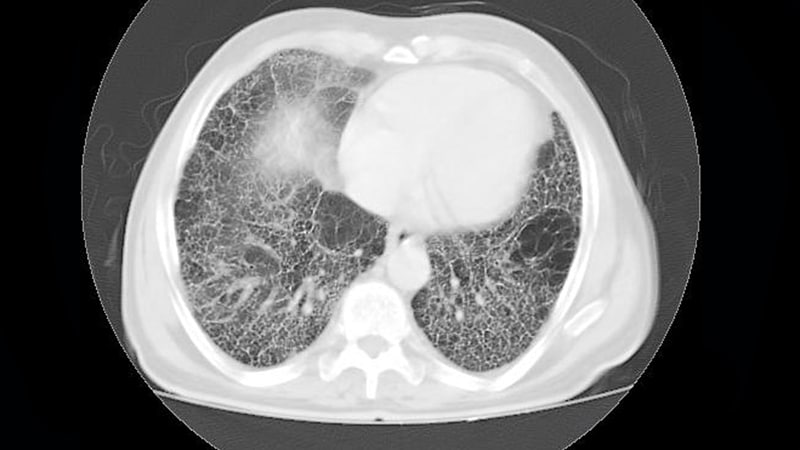
圣地亚哥 — 患者 特发性肺纤维化 (IPF) 经过 12 周的 Hedgehog 信号通路研究抑制剂治疗后,肺功能显着改善,肺纤维化逆转。 Toby 表示,2a 期安全性试验的早期疗效数据表明,这种名为 ENV-101 的新型口服药物与用力肺活量 (FVC) 和其他肺功能指标的改善相关,可能是 IPF 的一种疾病缓解疗法。 M. Maher,医学博士、哲学博士,洛杉矶南加州大学凯克医学院间质性肺疾病主任。 “从历史上看,我们并没有看到 FVC 的改善,但这正是我们所看到的 [with ENV-101],我认为可以重塑肺部早期纤维化区域,”马赫在接受采访时说。 “我们从组织学研究中知道,如果你观察 IPF 肺部,你会看到终末期纤维化的区域,但即使在晚期疾病中,你也会看到肺部保存相对完好且存在早期纤维化的区域,所以我认为可以想象,一些早期纤维化区域正在重塑,”他说。 重要途径 Hedgehog 通路在进化中高度保守。 细胞信号传导途径在胚胎发生、组织增殖和器官发育中活跃。 马赫解释说,还有证据表明,在成人中,该通路在组织损伤后重新激活,这可能发生在肺上皮细胞中。 尽管 IPF 中的“特发性”一词表明该疾病的病因尚不清楚; 研究人员发现,在 IPF 中,肺组织的重复上皮损伤会导致 Hedgehog 通路的激活。 Maher 说,Hedgehog 信号转而诱导肌成纤维细胞的形成和激活,从而形成纤维化基质并收缩肺组织,导致气体交换显着受损。 ENV-101 阻断 Hedgehog 与 PTCH1 受体的结合,从而阻止释放 锌-手指蛋白GLI1从激酶复合物进入细胞质。 当信号传导被阻断时,肌成纤维细胞会发生细胞凋亡,而不是启动细胞凋亡。 伤口修复 他解释说,就像平常一样,从而消除了 […]
重新利用人类批准的药物来治疗朊病毒病

朊病毒是可传播的异常致病因子,能够诱导特定正常细胞蛋白质的异常折叠。 朊病毒病是一组致命且目前无法治疗的神经退行性疾病的总称,这些疾病不仅影响人类,还影响野生和圈养动物。 这些疾病包括人类克雅氏病 (CJD)、牛海绵状脑病 (BSE,或“疯牛病”) 以及影响鹿、麋鹿和驼鹿的慢性消耗性疾病 (CWD)。 这些疾病的核心事件是朊病毒蛋白(PrPC)从其正常形状转变为对神经元有毒的病理结构(PrPSc),并且可以通过与未转变的 PrPC 分子结合来自我复制。 这种自我复制的能力使这些错误折叠的蛋白质具有传染性,这对公共健康具有巨大的影响。 在一项新研究中,波士顿大学 Chobanian & Avedisian 医学院的研究人员鉴定出 10 种能够降低受感染细胞中 PrPSc 水平的化合物,并表明最有效的分子还可以防止将 PrPSc 应用于培养细胞时观察到的毒性。神经元。 “令人兴奋的是,其中五种分子具有在人类中使用的历史:用于治疗神经精神疾病的林卡唑和氟哌啶醇,用于治疗神经性疼痛的 (+)-喷他佐辛,以及正在进行缺血性中风和阿尔茨海默病临床试验的 SA 4503 和 ANAVEX2-73 , 分别,” 主要作者、该校生物化学和细胞生物学讲师 Robert CC Mercer 博士解释道。 研究人员最初探索了这些分子的抗朊病毒特性,因为已知它们与西格玛受体(σ1R 和 σ2R)结合,他们有理由相信这些分子参与了朊病毒增殖。 利用基因敲除技术(CRISPR),从其抗朊病毒特性的角度来看,他们确定西格玛受体不是这些药物的相关靶点。 使用来自已感染朊病毒的实验模型的 Neuro2a 细胞 (N2a),然后将这些细胞暴露于浓度不断增加的每种药物中,并测定 PrPSc 的水平。 然后,他们使用 CRISPR 技术“编辑”σ1R 和 σ2R 基因,使它们不再编码蛋白质,并发现这对他们在应用药物时观察到的 PrPSc 水平下降没有影响。 这使他们得出结论,σ1R 和 […]
研究发现 COVID-19 与自身免疫性肺病的增加有关

最近 电子生物医学 研究确定了严重急性呼吸综合征冠状病毒 2 (SARS-CoV-2) 感染和黑色素瘤分化相关蛋白 5 (MDA5) 自身免疫之间共有的免疫病理学。 学习: 与 COVID-19 大流行同时发生的 MDA5-自身免疫和间质性肺炎 (MIP-C)。 图片来源:Light Studio Design / Shutterstock.com 背景 皮肌炎 (DM) 是一种自身免疫性疾病,其特征是严重的皮肤和肌肉炎症。 此外,DM 与间质性肺病 (ILD) 有关,后者会导致进行性肺纤维化。 临床上,无肌病性皮肌炎 (CADM) 与 DM 显着相关,并导致进行性 ILD。 CADM 通过视黄酸诱导基因 1 (RIG-1) 样受体家族基因 IFIH1 表达,该基因编码 MDA5 蛋白。 最近的一项研究强调,2019 年冠状病毒病 (COVID-19) 大流行之前的 MDA5+ 病例表现出 ILD 的显着表现。 然而,这些患者并没有出现典型的 DM 向日光性皮疹,而是出现了基于皮肤的临床症状,包括触痛的手掌丘疹和皮肤溃疡。 MDA5 […]
关于新型精神分裂症的“令人印象深刻”的新数据充满希望 KarXT

EMERGENT-3 试验的结果证实,新型在研抗精神病药物 xanomeline-trospium(KarXT,Karuna Therapeutics)对成人患者有效且耐受性良好 精神分裂症 经历急性精神病。 EMERGENT-3 的研究结果与 EMERGENT-1 和 EMERGENT-2 的研究结果相结合,“支持 xanomeline-trospium 成为推定的不含 D2 的新型抗精神病药物中第一个的潜力 多巴胺 受体阻断活性,”由 Karuna Therapeutics 的医学博士、公共卫生硕士 Inder Kaul 领导的作者写道。 “EMERGENT-3 与安慰剂相比,总体精神病理学改善效果为 0.60,令人印象深刻,并且与之前的研究结果一致,”Hofstra/Zucker 医学院精神病学教授 Christoph U. Correll 博士说。纽约市诺斯韦尔告诉 Medscape 医学新闻。 Correll 说:“同样令人鼓舞的是,它的安全性并不包括我们所习惯的通常的集群,尽管在不同程度上是目前可用的多巴胺受体阻滞剂。”Correll 参与了 EMERGENT-2 但没有参与 EMERGENT-3。 EMERGENT-2 的结果是 去年年底发表 在 柳叶刀。 EMERGENT-3 结果是 5月1日在线发布 在 《美国医学会杂志》精神病学。 临床上有意义的改善 EMERGENT-3 招募了来自美国和乌克兰 30 个住院点的 […]
研究表明奶牛的乳腺中同时含有人类和禽流感受体

在最近发布的一项研究中 生物Rxiv 在预印本*服务器上,研究人员使用凝集素组织化学来评估甲型流感病毒 (IAV) 受体在牛呼吸系统、大脑和乳腺中的原位表达。 学习: 禽类和人类甲型流感病毒受体唾液酸 (SA)-α2,3 和 SA-α2,6 在牛乳腺中广泛表达。 图片来源:Arie van der Wulp / Shutterstock 背景 在美国奶牛中发现了高致病性 IAV (HPIAV) 流行,奶牛是一种相对未知的国内 IAV 宿主物种。 IAV 是一种负义单链核糖核酸 (RNA) 病毒,尚未在牛中引起广泛感染。 牛主要对 IAV 具有免疫力,但容易受到丙型和丁型流感病毒的感染。 然而,高致病性禽流感病毒 (HPAIV) H5N1 在德克萨斯州被发现,并迅速传播到美国八个州的 40 多个牛群。 临床指标包括产奶量突然下降、乳腺炎、中度呼吸道症状以及感染 2.3.4.4b 病毒的其他哺乳动物所没有的神经系统症状。 关于该研究 在本研究中,研究人员检查了 IAV 受体表达 现场 存在于牛的乳腺、呼吸道和大脑中,被认为不易受到 IAV 感染。 研究人员从两只2.0个月大的小牛身上获取了气管和肺部标本,其中一头患有严重的化脓性气管炎。 他们在丹麦哥本哈根大学兽医病理学部门定期尸检时收集了各种临床患者的组织。 他们从一头哺乳奶牛(四岁)身上获得了两个无病的乳腺。 他们从一头 5 个月大的肉牛犊和一头 2.5 […]
肠道微生物组中的天然化合物显示出治疗炎症的希望
多伦多大学的研究人员发现肠道中天然存在的化合物可以用来减少炎症和其他消化问题症状。 这可以通过将化合物与重要但知之甚少的核受体结合来实现。 肠道微生物群中含有细菌,这些细菌会产生化合物,这些化合物是我们以消化残渣为食的副产品。 这些化合物可以与核受体结合,帮助转录 DNA 产生蛋白质和非编码 RNA 片段。 通过确定哪些微生物副产物可以用来调节受体,研究人员希望挖掘它们治疗疾病的潜力。 我们对人类肠道微生物群中的小分子进行了公正的筛选。 我们发现这些分子的作用与目前用于调节组成型雄甾烷受体(也称为 CAR)的人工化合物类似。 这使它们成为药物开发的可行候选者。” Jiabao Liu,该研究的第一作者,多伦多大学唐纳利细胞和生物分子研究中心的研究员 该研究最近发表在 自然通讯杂志。 CAR 在调节肝脏内异物(包括药物)的分解、吸收和清除方面发挥着关键作用。 它还与肠道炎症有关。 Henry Krause 说:“研究 CAR 的挑战之一是,没有一种有用的化合物能够同时与人类和小鼠版本的受体结合——后者对于在人体测试之前进行研究和疾病建模是必要的。”该研究的首席研究员,唐纳利中心和特默蒂医学院的分子遗传学教授。 “之前的努力集中在开发具有强大结合和激活能力的分子。这导致合成调节剂过度激活受体,从而可能导致意想不到的结果。我们发现的天然化合物不会导致这个问题。” 这两种化合物可调节人和小鼠肝脏中的 CAR。 它们还被发现与名为 CITCO 的人造人类 CAR 调节器的有效性相匹配。 未来 CAR 调节研究的一个有希望的发现是,这两种化合物都不会对小鼠产生副作用,例如肝脏肿大。 这意味着 DIM 和 DIE 可用于研究小鼠的 CAR 功能和调节,并将研究结果应用于人类。 “这种受体在糖尿病、脂肪肝和小肠溃疡性结肠炎中发挥作用,”刘说。 “我们可以用我们发现的人类肠道中已经存在的两种天然化合物来治疗所有这些问题。” 这项研究得到了国家研究院、美国癌症协会、加拿大健康研究院、美国国立卫生研究院、加拿大自然科学和工程研究委员会以及新前沿研究基金的支持。 来源: 期刊参考: 刘,J., 等人。 (2024)。 由共生微生物代谢物产生的二吲哚充当内源性 CAR/Nr1i3 配体。 自然通讯。 […]
PPI 与偏头痛和其他严重头痛类型有关
新研究表明,用于控制胃酸反流的质子泵抑制剂(PPI)会增加偏头痛和其他严重头痛类型的风险。 研究人员利用国家健康和营养检查调查 (NHANES) 的数据进行了横断面分析,发现所有类型的抑酸疗法都与包括偏头痛在内的严重头痛风险增加相关,但 PPI 带来的风险最大。 “值得注意的是,许多人确实需要减酸药物来控制胃酸反流或其他病症,而正在服用这些药物或补充剂的偏头痛或严重头痛的人应该与医生讨论是否应该继续服用,”主要作者马里兰大学帕克分校的玛格丽特·斯莱文 (Margaret Slavin) 博士在一份报告中表示 新闻稿。 研究结果是 在线发布 2024 年 4 月 24 日,于 神经病学临床实践。 旧数据的新视角 先前的研究表明,头痛是服用 PPI 和组胺受体激动剂 (H2RA) 的成人最常见的不良反应之一,其中包括 西咪替丁, 法莫替丁和 尼扎替丁。 其他大型健康数据库研究表明,接触 PPI 一周内头痛风险增加。 为了比较 PPI 与 H2RA 的风险,其他研究人员分析了 NHANES 中使用 PPI、H2RA 和普通抗酸剂的患者的数据,以了解更多关于抑酸疗法和头痛之间的潜在联系。 他们使用了 1999 年至 2004 年的调查数据,这是 NHANES 在过去 3 个月内唯一包含有关偏头痛和其他头痛问题的年份。 研究人员分析了 11,800 名年龄 ≥ 20 […]
研究确定白血病如何对一线治疗产生耐药性
%2c_analyze_by_microscope-Jarun_Ontakrai_8864dd9cfb3b4dff9a913aede7a7c915-620x480.jpg)
一项新的研究确定了癌症如何对一线治疗产生耐药性,这种常见形式的白血病复发可能是可以预防的。 新研究发表于 科学 来自伯明翰大学、癌症研究所 (ICR)、纽卡斯尔大学、马克西玛公主儿科肿瘤中心和弗吉尼亚大学的研究人员发现了复发患者的急性髓性白血病 (AML) 样本突变形式的变化接受FLT3抑制剂治疗后。 研究小组发现,耐药性癌症上调了多种其他信号通路来克服药物的作用,并且这种基因变化能够在实验室测试中复制。 这些实验表明,通过靶向 RAS 家族蛋白,使用牛津大学韦瑟罗尔分子医学研究所和 ICR 的 Terry Rabbitts 团队通过化学库筛选开发的小分子抑制剂,该抑制剂使用抑制性细胞内抗体的互补位,增强了信号传导不再将细胞从细胞死亡中拯救出来。 研究小组发现转录因子 AP-1 和 RUNX1 是介导耐药性的核心。 这两个因子协同作用并与其靶基因结合在一起,但前提是存在生长因子信号传导。 针对 FLT3 的药物重新连接细胞,导致其他信号通路相关基因的上调,然后恢复 AP-1 和 RUNX1 的结合。 RAS 是多种信号传导途径的关键组成部分,药物阻止了 RUNX1 结合的恢复,因此来自生长因子的信号传导不再能拯救癌细胞免于死亡。 刚刚到墨尔本大学任职、伯明翰大学癌症与基因组科学研究所的 Constanze Bonifer 教授是该论文的资深作者之一,他表示: ”制药行业对针对异常生长因子受体(例如 FLT3-ITD)的药物能够防止人们复发寄予厚望。 然而,癌细胞很聪明,会重新连接它们的生长控制机制,以利用体内存在的其他生长因子。 针对 RAS 家族成员可防止癌症重新布线并使用不同的信号通路来逃避细胞死亡”。 以 RAS 为目标会阻止重新布线 本研究中用于靶向 RAS 的小分子抑制剂是利用细胞内抗体技术开发的。 该技术涉及筛选大量抗体片段,以识别那些与细胞中的靶蛋白结合并阻止其蛋白质-蛋白质相互作用的抗体片段。 可以从与这些抗体片段结合的靶蛋白部分(互补位)相互作用的化学文库中筛选小分子抑制剂。 由于这些抗体片段无与伦比的天然特异性,该技术(称为 A恩蒂乙奥迪 derived 或 […]
研究人员发现了一种有前途的方法来去除阿尔茨海默病中的淀粉样斑块
阿尔茨海默病始于一种称为β淀粉样蛋白的粘性蛋白,它在大脑中积聚成斑块,引发一系列事件,导致大脑萎缩和认知能力下降。 新一代阿尔茨海默病药物——; 第一个被证明可以改变病程的-; 通过标记淀粉样蛋白以供大脑免疫细胞清除来发挥作用。 现在,圣路易斯华盛顿大学医学院的研究人员发现了一种不同的、有前途的方法来去除有害斑块:直接动员免疫细胞消耗它们。 4 月 3 日发表在《 科学转化医学研究人员表明,用抗体激活称为小胶质细胞的免疫细胞可以减少大脑中的淀粉样斑块,并减轻患有阿尔茨海默病样疾病的小鼠的行为异常。 这种方法的影响可能不仅仅局限于阿尔茨海默病。 脑蛋白的有毒团块是许多神经退行性疾病的特征,包括帕金森病、肌萎缩侧索硬化症 (ALS) 和亨廷顿舞蹈病。 受到研究结果的鼓舞,研究人员正在探索其他潜在的免疫疗法(利用免疫系统的药物),以清除大脑中被认为会促进其他疾病的垃圾蛋白。 该研究的资深作者、Robert Rock Belliveau 医学博士 Marco Colonna 解释说:“通过普遍激活小胶质细胞,我们的抗体可以清除小鼠体内的淀粉样蛋白斑块,并且有可能清除其他神经退行性疾病(包括帕金森氏病)中的其他破坏性蛋白质。”医学博士,病理学教授。 小胶质细胞围绕斑块形成屏障,控制破坏性蛋白质的扩散。 它们还可以吞噬并破坏斑块蛋白,但在阿尔茨海默病中它们通常不会。 它们的被动性可能来自一种称为 APOE 的蛋白质,它是淀粉样斑块的组成部分。 该研究的共同第一作者 Yun Chen 解释说,斑块中的 APOE 蛋白与斑块周围小胶质细胞上的受体 LILRB4 结合,使它们失活。 由于尚不清楚的原因,研究人员发现,在患有阿尔茨海默病的小鼠和人中,斑块周围的小胶质细胞会产生 LILRB4 并将其定位在细胞表面,这会抑制它们在与 APOE 结合后控制破坏性斑块形成的能力。 另一位共同第一作者侯金超博士(现为中国浙江省浙江大学医学院附属儿童医院的一名教员)用一种自制抗体治疗大脑中存在β淀粉样蛋白斑块的小鼠,该抗体可阻止 APOE 与LLRB4。 在与华盛顿大学马林克罗特放射学研究所放射学教授 Yongjian Liu 博士合作确认抗体到达大脑后,研究人员发现激活的小胶质细胞能够吞噬并清除淀粉样蛋白斑块。 清除小鼠的β淀粉样蛋白斑块也可以减轻冒险行为。 患有 AD 的人可能缺乏对过去经历的记忆来指导他们的决定。 他们可能会从事危险行为,从而容易成为欺诈或财务滥用的受害者。 用抗体治疗小鼠以清除斑块,有望改变小鼠的行为。 大脑中形成β淀粉样蛋白斑块后,另一种大脑蛋白质-; τ-; […]
研究发现DNA修复过程是记忆形成的关键
在最近发表在该杂志上的一项研究中 自然研究人员发现,在学习过程中诱发一系列分子事件之前,神经元被招募到记忆回路中,其中包括海马神经元簇中的双链脱氧核糖核酸(DNA)损伤以及由 Toll 样受体 9(TLR9)介导的修复。 学习: 通过 DNA 传感 TLR9 通路形成记忆组件。 图片来源:十亿照片/Shutterstock 背景 当海马体中的神经元经历长期的分子适应以形成皮质微电路以响应刺激时,记忆就形成了。 这个过程是能源密集型的,并且涉及大量的形态和生化变化。 这些分子变化被认为会导致双链 DNA 短暂断裂。 研究还探索了内在神经元和预先存在的发育程序在记忆形成中的作用,并发现环磷酸腺苷 (cAMP) 反应元件结合蛋白 (CREB) 等转录因子参与了该过程。 最近的研究还集中于了解神经元间神经元周围网络如何控制神经元组件的抑制输入以稳定记忆回路。 关于该研究 在本研究中,研究人员试图理解和识别任何整合预先存在的发育机制和刺激启动途径的总体过程,这些过程影响神经元参与特定于记忆的组装或微电路。 使用小鼠模型来分析背海马区域神经元的转录谱超过 48 小时,以了解即时、早期和延迟的基因表达和蛋白质信号传导。 在这项分析中,小鼠接受情境恐惧调节,并且在调节后 4 或 21 天获得的海马样本用于大量核糖核酸 (RNA) 测序。 鉴于已知在神经元活动期间会诱导双链 DNA 的短暂断裂,从而诱导立即早期基因表达,他们假设学习活动引起的 DNA 损伤可能在离散的神经元群体中更广泛和持续。 使用磷酸组蛋白 γH2AX 与双链 DNA 断裂结合的特异性抗体进行免疫荧光标记,以了解情境恐惧调节产生的核外双链 DNA 片段的起源。 情境恐惧调节一小时后还收集了脑切片,以分析与早期基因表达相关的 γH2AX 信号。 此外,还使用免疫染色分析了 CREB 的基线表达,该表达已被确定在记忆中发挥作用。 研究人员还研究了记忆重新激活过程中 […]
