运动有助于消除 PTSD 患者的记忆

概括: 在运动或基因操作的刺激下,海马体中神经元形成的增加可以帮助小鼠忘记创伤或与药物相关的记忆。 这个过程涉及重新连接神经回路,扰乱恐惧记忆的回忆。 这些发现为治疗创伤后应激障碍和毒瘾等心理健康问题提供了潜在的新方法。 主要事实: 运动和基因操作会增加海马体中神经元的形成。 神经发生的增加导致神经回路的重新布线和恐惧记忆的遗忘。 这一发现可能会带来治疗创伤后应激障碍和毒瘾的新疗法。 加拿大多伦多大学和日本九州大学的研究人员发现,通过锻炼或基因操作,海马体中神经元形成的增加以及随后神经回路的重新布线有助于小鼠忘记创伤或与药物相关的记忆。 调查结果于 5 月 8 日发表在 分子精神病学, 可以提供一种治疗创伤后应激障碍(PTSD)或毒瘾等心理健康问题的新方法。 创伤后应激障碍(PTSD)是一种心理健康状况,可能因经历或看到创伤事件(例如自然灾害、严重事故或袭击)而引发。 在全球范围内,大约 3.9% 的总人口患有创伤后应激障碍 (PTSD),其症状包括生动的闪回和回避行为,例如远离那些让他们想起创伤事件的地方或推开那些让他们想起创伤事件的人。 研究人员随后探讨了是否可以通过锻炼来缓解这些类似创伤后应激障碍的行为,研究表明锻炼可以促进神经发生。 目前,创伤后应激障碍通常通过治疗或抗抑郁药等药物来治疗,但由于许多人没有有效的反应,研究人员仍在寻找不同的治疗方法。 在这项针对小鼠的研究中,九州大学药学院的助理教授 Risako Fujikawa、她的前导师、多伦多大学的 Paul Frankland 教授以及包括 Adam Ramsaran 在内的团队成员重点研究了神经发生(形成新神经元的过程)如何在小鼠中发挥作用。海马体影响忘记恐惧记忆的能力。 海马体是大脑中的一个区域,对于形成与特定地点和环境相关的记忆非常重要,每天都会在齿状回区域产生新的神经元。 “神经发生对于形成新记忆很重要,但对于遗忘记忆也很重要。 我们认为发生这种情况是因为当新的神经元整合到神经回路中时,新的连接就会形成,旧的连接就会丢失,从而破坏了回忆的能力,”藤川解释道。 “我们想看看这个过程是否也能帮助老鼠忘记更强烈的创伤记忆。” 研究人员在不同的环境下对小鼠进行了两次强烈的电击。 首先,老鼠离开一个明亮的白色盒子并进入一个黑暗的、有乙醇气味的隔间后感到震惊。 在另一个不同环境中进行第二次电击后,小鼠表现出类似创伤后应激障碍的行为。 一个多月后,小鼠仍对进入原来的暗室感到恐惧和犹豫,表明它们无法忘记创伤记忆。 这种恐惧延伸到了其他黑暗的隔间,表现出普遍的恐惧。 此外,小鼠在开放空间的探索较少,并避开中心,这表明它们感到焦虑。 研究人员随后探讨了是否可以通过锻炼来缓解这些类似创伤后应激障碍的行为,研究表明锻炼可以促进神经发生。 双重电击的小鼠被分成两组,其中一组配有跑轮。 四个星期后,这些小鼠的海马体中新形成的神经元数量有所增加,重要的是,与没有轮椅通道的双重电击小鼠相比,类似 PTSD 的行为不那么严重。 此外,当小鼠在第二次电击前自由运动时,也可以防止一些类似创伤后应激障碍的行为的发生。 然而,由于运动以多种不同的方式影响大脑和身体,目前尚不清楚运动的影响是由于神经发生或其他因素导致的海马回路重新布线。 因此,研究人员使用两种不同的遗传方法来专门评估新生神经元整合到海马体中的影响。 首先,研究人员使用了一种称为光遗传学的技术,他们将光敏蛋白添加到齿状回新形成的神经元中,使神经元能够被光激活。 当他们用蓝光照射这些细胞时,新的神经元成熟得更快。 14天后,神经元变得更长,有更多分支,并且更快地整合到海马体的神经回路中。 在第二种方法中,研究小组利用基因工程去除了新形成的神经元中一种减缓神经元生长的蛋白质。 这也导致神经元生长得更快,并更多地融入神经回路。 […]
环绕脊髓装置可能会改变损伤治疗
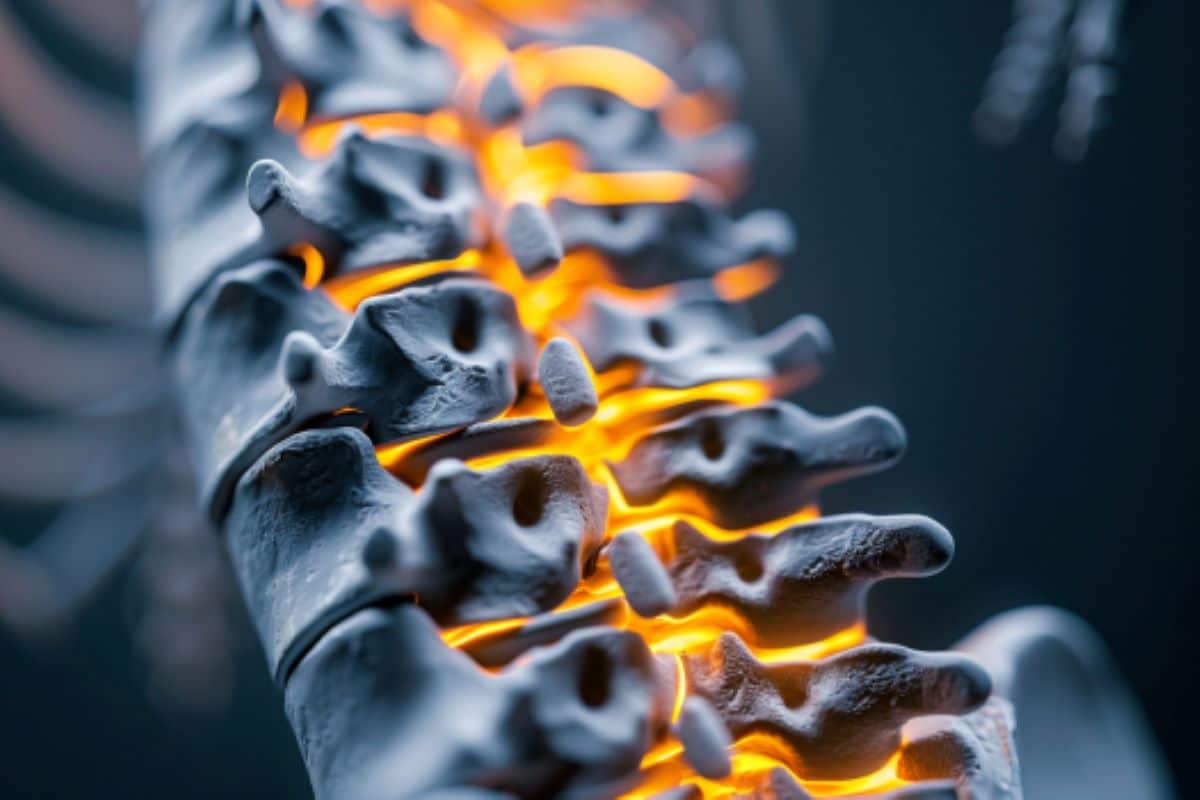
概括: 研究人员开发了一种突破性的电子设备,可以包裹脊髓,为治疗脊髓损伤提供了一种无需进行脑部手术的新方法。 该设备可以记录和刺激整个脊髓的神经信号,提供完整的 360 度脊柱活动视图。 在对动物模型和人类尸体的测试中,它证明了它能够刺激肢体运动并绕过脊髓受损区域。 这项创新技术避免了与传统植入方法相关的高风险,也有望改善手术监测和对脊柱状况的了解。 关键事实: 与捕获有限脊髓区域的传统方法不同,该设备提供脊髓活动的完整 360 度映射。 它已在动物试验中成功刺激肢体运动,并已被证明适用于人体模型。 该技术避免了脑部手术和直接穿透脊髓,从而降低了进一步受伤的风险。 一种包裹脊髓的微型柔性电子设备可能代表一种治疗脊柱损伤的新方法,脊柱损伤可能导致严重的残疾和瘫痪。 剑桥大学的工程师、神经科学家和外科医生团队开发了这些设备,并用它们记录大脑和脊髓之间来回的神经信号。 虽然此类治疗至少还需要几年的时间,但研究人员表示,这些设备在短期内可能有助于监测手术期间的脊髓活动。 图片来源:神经科学新闻 与目前的方法不同,剑桥设备可以记录 360 度信息,提供脊髓活动的完整图像。 在活体动物和人体尸体模型中进行的测试表明,这些设备还可以刺激肢体运动并绕过完全脊髓损伤(即大脑和脊髓之间的通讯完全中断)。 目前治疗脊柱损伤的大多数方法都涉及用电极刺穿脊髓和在大脑中植入植入物,这都是高风险的手术。 剑桥大学开发的设备可以治疗脊柱损伤,而无需进行脑部手术,这对患者来说更加安全。 虽然此类治疗至少还需要几年的时间,但研究人员表示,这些设备在短期内可能有助于监测手术期间的脊髓活动。 更好地了解脊髓是很难研究的,可以改善对一系列疾病的治疗,包括慢性疼痛、炎症和高血压。 结果发表在期刊上 科学进步。 “脊髓就像一条高速公路,以神经冲动的形式将信息传入和传出大脑,”这项研究的共同领导者、工程系教授乔治·马利亚拉斯 (George Malliaras) 说。 “脊髓损伤会导致交通中断,导致严重残疾,包括不可逆转的感觉和运动功能丧失。” 监测进出脊髓的信号的能力可以极大地帮助开发脊髓损伤的治疗方法,并且在近期内也可以用于在手术期间更好地监测脊髓。 “大多数用于监测或刺激脊髓的技术仅与脊髓背部或背侧部分的运动神经元相互作用,”该研究的共同领导者、临床神经科学系的达米亚诺·巴罗内博士说。 “这些方法只能到达脊柱的 20% 到 30%,所以你得到的图像并不完整。” 研究人员从微电子学中汲取灵感,开发出一种从整个脊柱获取信息的方法,即在脊髓周围包裹非常薄的高分辨率植入物。 这是首次实现脊髓的安全 360 度记录——早期的 360 度监测方法使用刺穿脊柱的电极,这可能会导致脊髓损伤。 剑桥开发的生物相容性设备厚度仅为百万分之几米,采用先进的光刻和薄膜沉积技术制成,只需极小的电力即可运行。 这些设备拦截在脊髓的轴突或神经纤维上传播的信号,从而可以记录信号。 这些设备很薄,意味着它们可以记录信号而不会对神经造成任何损害,因为它们不会穿透脊髓本身。 “这是一个困难的过程,因为我们以前没有以这种方式制造过脊柱植入物,而且不清楚我们是否可以安全、成功地将它们放置在脊柱周围,”马利亚拉斯说。 “但由于工程和神经外科领域的最新进展,行星已经对齐,我们在这个重要领域取得了重大进展。” 这些装置是根据常规外科手术进行改造而植入的,因此它们可以滑入脊髓下方而不会损坏脊髓。 在使用大鼠模型的测试中,研究人员成功地使用这些设备来刺激肢体运动。 这些设备表现出非常低的延迟——也就是说,它们的反应时间接近人类的反射性运动。 人体尸体模型的进一步测试表明,该设备可以成功地植入人体。 研究人员表示,他们的方法可能会改变未来脊柱损伤的治疗方式。 目前治疗脊柱损伤的尝试涉及大脑和脊柱植入物,但剑桥研究人员表示,大脑植入物可能没有必要。 […]
脑癌免疫疗法的突破
概括: 研究人员推出了一种新的联合免疫疗法,可显着增强恶性胶质瘤患者的免疫反应。 通过将个性化树突状细胞疫苗与免疫增强剂poly-ICLC相结合,该疗法有望增强树突状细胞对抗这种侵袭性脑肿瘤的能力。 这一进展为恶性神经胶质瘤患者带来了新的希望,由于恶性神经胶质瘤的快速生长和浸润脑组织,治疗起来非常困难。 该研究强调了这种联合疗法彻底改变治疗模式并改善恶性神经胶质瘤病例的患者预后的潜力。 主要事实: 增强免疫反应: 研究发现,树突状细胞疫苗与聚 ICLC 的组合可显着增强免疫系统的反应,提高 T 细胞对抗恶性神经胶质瘤的活性和功效。 创新方法: 该疫苗利用患者自身的白细胞,经过修饰后可以识别和攻击脑肿瘤细胞,并通过添加聚 ICLC 进行放大,以增强免疫反应。 有希望的结果: 初步研究结果表明,这种疗法不仅提高了免疫系统对抗肿瘤的能力,而且还表明有可能延长患者的生存期,需要进一步的研究来证实这些结果。 加州大学洛杉矶分校健康琼森综合癌症中心的研究人员找到了一种联合免疫疗法,可以增强恶性胶质瘤患者的免疫反应,恶性胶质瘤是一种生长迅速且难以治疗的侵袭性脑肿瘤。 该研究发表于 自然通讯研究发现,个性化树突状细胞疫苗与免疫增强物质poly-ICLC配对,可以增强恶性胶质瘤患者的免疫反应和T细胞活性,比单独使用疫苗更有效地提高树突状细胞对抗脑肿瘤的能力。 治疗后对干扰素没有反应或表现出低干扰素反应的患者可以更快地接受其他治疗或临床试验,从而在对抗这种侵袭性脑癌的过程中节省宝贵的时间。 图片来源:神经科学新闻 “恶性胶质瘤的治疗非常复杂,由于这些肿瘤的浸润性及其在大脑中的位置,这些患者的预后往往很差,”大卫格芬大学分子和医学药理学以及神经外科教授罗伯特·普林斯(Robert Prins)说。加州大学洛杉矶分校医学院,该研究的共同高级作者。 “通过提高疫苗的效力,我们希望它能够在诊断为恶性神经胶质瘤的患者中诱导更有效的抗肿瘤免疫反应。” 加州大学洛杉矶分校首创的树突状细胞疫苗利用人自身的白细胞来帮助激活免疫系统来对抗癌症。 当树突状细胞检测到外来入侵者时,通常会向免疫系统发出警报。 该疫苗的工作原理是将手术切除的肿瘤产生的脑肿瘤蛋白抗原与患者自身血液产生的树突状免疫细胞结合起来。 树突状细胞训练免疫系统识别肿瘤抗原,这样当它们被注射回患者体内时,免疫系统将被训练识别并攻击肿瘤细胞。 虽然疫苗在治疗恶性神经胶质瘤患者方面显示出希望,但这种治疗方法并不适合所有人。 为了进一步增强抗肿瘤免疫反应,研究人员考虑在疫苗中添加 Toll 样受体 (TLR) 激动剂。 TLR 激动剂结合并激活树突状细胞和巨噬细胞表达的进化保守受体家族,帮助免疫系统对外来病原体发出警报。 通过激活树突状细胞上的这些 TLR,加州大学洛杉矶分校团队推测,这种组合可能会增加抗肿瘤特异性 T 细胞的频率和浸润,同时降低肿瘤微环境的抑制能力。 研究小组专门研究了两种不同的 TLR 激动剂——聚 ICLC 和瑞西莫德——以确定哪一种与疫苗联合使用更安全、更有效。 该团队招募了 23 名年龄从 26 岁到 72 岁不等的 WHO […]
让我们谈谈:基于网络的聊天可增强老年人的大脑功能

概括: 基于互联网的对话可以显着改善社交孤立的老年人的认知功能。 这项名为 I-CONECT 的试验涉及 186 名年龄在 75 岁及以上的参与者,他们每周进行四次结构化视频聊天,这有助于增强记忆力和执行功能,特别是对于那些患有轻度认知障碍的人。 在一年的时间里,这些互动不仅提高了认知分数,还改善了情绪健康,并增强了与注意力相关的大脑区域的连通性。 研究结果表明,数字对话可以成为对抗社会孤立及其认知影响的可行策略。 关键事实: 增强认知功能:I-CONECT 试验中经常进行数字对话的参与者表现出整体认知测试分数和基于语言的执行功能的改善。 改善情绪健康:对照组和干预组的情绪健康状况均得到改善,这表明定期的社交接触,即使是短暂的,也可以产生积极的影响。 神经系统的好处:大脑成像显示干预组的背侧注意力网络内的连接性增加,突出了对话互动增强大脑功能的潜力。 根据马萨诸塞州总医院的一项新的临床试验,即使互动是基于互联网的,与其他人交谈也可以刺激社交孤立的老年人的不同大脑功能。 结果发表于 老年学家。 主要作者、首席研究员 Hiroko H. Dodge 解释道:“我们于 2010 年启动了第一项概念验证行为干预研究,比 COVID-19 大流行早了近十年,引起人们对社会隔离对我们整体健康的不利影响的关注。”美国国立卫生研究院资助的试验。 对照组和干预组的情绪健康指标均有所改善,这表明每周简短的电话通话可以提高情绪,而改善认知功能则需要频繁的对话参与。 图片来源:神经科学新闻 这项名为 I-CONECT 的 186 名参与者的 2 期随机试验使用互联网和网络摄像头,允许受过训练的采访者与 75 岁及以上、认知正常或轻度认知障碍、与社会隔离的个体之间进行对话互动。 研究人员轮换分配给每个参与者的对话伙伴,以增强体验的新颖性,提供用户友好的设备,让没有任何互联网/网络摄像头经验的参与者轻松参与基于视频的对话,并鼓励使用标准化的日常主题和图片提示进行对话。 六个月内每周进行四次三十分钟的对话,然后再进行六个月每周两次。 由类似个体组成的对照组没有参与此类对话,但干预组和对照组每周都会接受 10 分钟的电话检查。 在最初的六个月后,与对照组相比,干预组的整体认知测试得分更高,并且在轻度认知障碍患者中效应量较大。 此外,认知正常的干预组参与者的得分表明基于语言的执行功能较高。 对照组和干预组的情绪健康指标均有所改善,这表明每周简短的电话通话可以提高情绪,而改善认知功能则需要频繁的对话参与。 应前试验参与者要求持续对话的要求,道奇和她的同事成立了一个非营利组织:I-CONNECT 基金会。 该基金会一直使用试验中使用的相同材料,免费为社区中孤立的老年人提供社交互动。 道奇说:“我们的下一个目标是将这些活动扩展到更多有需要的孤立个体,并深入研究社交互动对我们大脑功能影响的生物机制。” “通过互联网提供频繁的刺激性对话互动可能是一种有效的家庭痴呆症风险降低策略,可防止社会孤立和认知能力下降。 “我们计划将这种疗法扩展到老年门诊患者群体,目前我们正在为此筹集资金,并检查其对轻度至中度抑郁症状的有效性。” 该团队还在探索通过聊天机器人(一种经过人工智能训练的机器人)提供对话交互的可能性,它提供刺激的对话作为一种经济高效的干预措施。 “我们知道,人与人之间的接触对于我们的情绪健康至关重要,但对于认知刺激而言,聊天机器人可能会像人类一样有效地工作,我们目前正在对此进行研究,”道奇说,他担任该公司的研究分析总监。最近在 […]
基因疗法减缓 ALS 进展
概括: 研究人员利用一种新的基因疗法在 ALS 治疗方面取得了重大突破,标志着侵袭性 ALS 患者的疾病进展速度明显减慢。 该患者自 2020 年初以来接受治疗,大部分身体和社交能力均保持不变,超出了其病情的典型预期寿命和功能预测。 该疗法针对 SOD1 基因突变,降低有害蛋白质的水平并稳定患者的病情。 这些发现为 ALS 治疗的未来进步和基因治疗的更广泛应用带来了希望。 主要事实: 有效的基因治疗:该疗法显着降低与 ALS 相关的 SOD1 蛋白水平,从而减缓疾病进展。 显着的患者治疗效果:诊断四年后,患者继续独立进行日常活动,这对于患有侵袭性 ALS 的患者来说是一项罕见的成就。 FDA 和 EMA 批准:该药物已获得 FDA 批准,并被 EMA 推荐用于 SOD1 基因突变患者,表明其疗效和潜力。 肌萎缩侧索硬化症(ALS)疾病的研究取得突破。 于默奥大学的科学家报告称,使用一种新的基因疗法,患有特别侵袭性 ALS 疾病的患者的疾病进展已大大减慢。 经过四年的药物治疗后,患者仍然可以爬楼梯、从椅子上站起来、正常饮食和说话,并过着积极和社交充实的生活。 “我认为这是我们在默奥大学和北瑞典大学医院进行了 30 多年研究的突破。 于默奥大学临床科学系神经学家兼教授彼得·安德森 (Peter Andersen) 说:“使用任何其他治疗方法,我们以前从未见过如此有效的治疗结果。” ALS 疾病有多种类型,只有 2% 至 6% 的 ALS 疾病是由 SOD1 […]
关于阿尔茨海默氏症蛋白质积累的新见解
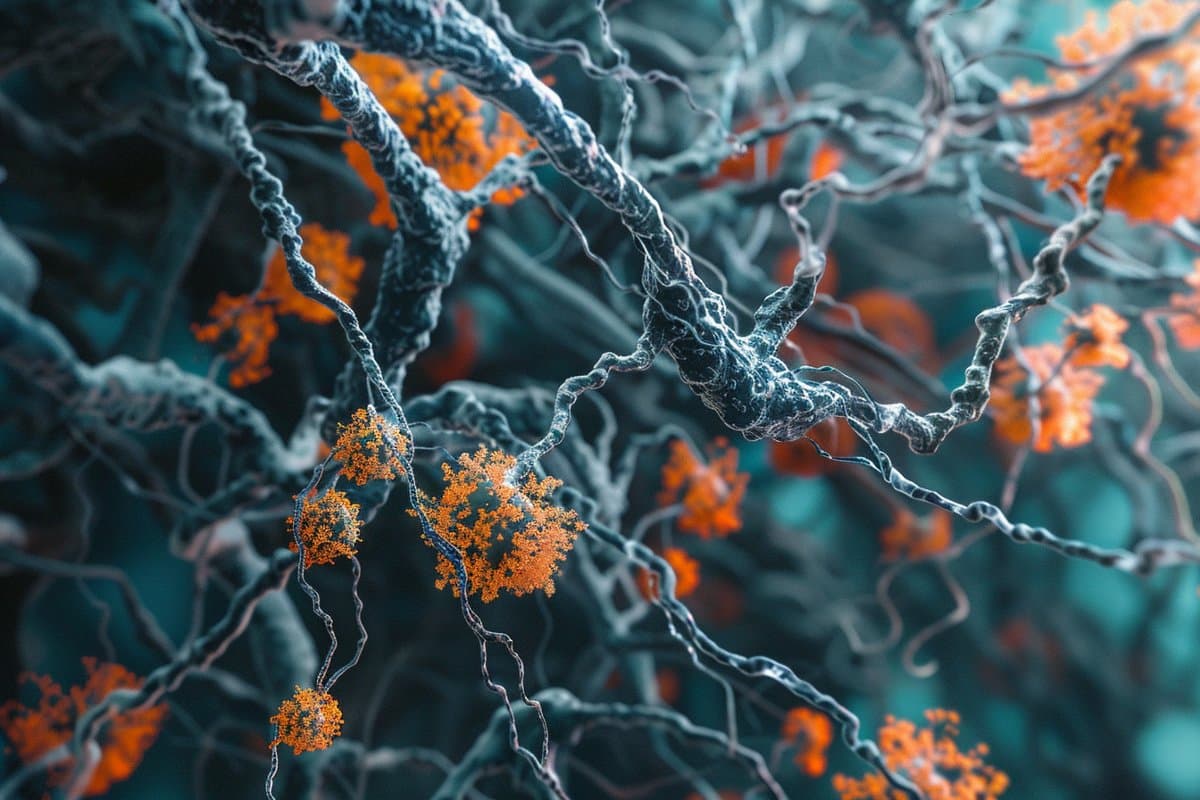
概括: 研究人员在了解阿尔茨海默氏症等神经退行性疾病中蛋白质积累背后的机制方面取得了重大发现。 通过研究果蝇,研究小组发现神经元轴突内线粒体的减少直接导致这种有害的蛋白质堆积。 他们指出蛋白质 eIF2β 的增加是一个关键因素; 降低其水平可以恢复蛋白质循环并改善神经元功能。 这一突破为治疗阿尔茨海默氏症和肌萎缩性脊髓侧索硬化症等疾病的治疗提供了新的目标,有可能改善患者的治疗结果。 关键事实: 研究表明,神经元轴突中线粒体的消耗会导致蛋白质异常积累,这是阿尔茨海默病等疾病的标志。 研究人员发现,蛋白质 eIF2β 的增加是这一过程的关键因素; 调整其水平可以扭转影响。 这些来自果蝇基因研究的发现为开发新疗法打开了大门,这些新疗法可以针对线粒体健康或调节蛋白质水平来对抗神经退行性疾病。 东京都立大学的研究人员发现了蛋白质如何在神经元中异常聚集,这是阿尔茨海默病等神经退行性疾病的一个特征。 他们利用果蝇来证明轴突中线粒体的消耗可以直接导致蛋白质积累。 同时,还发现了显着大量的一种名为 eIF2β 的蛋白质。 将水平恢复到正常会导致蛋白质回收的恢复。 这些发现有望为神经退行性疾病提供新的治疗方法。 众所周知,轴突中的线粒体水平会随着年龄的增长以及神经退行性疾病的进展而下降。 图片来源:神经科学新闻 我们体内的每个细胞都是一个忙碌的工厂,蛋白质不断地被生产和分解。 生产或回收阶段的任何变化或失误都可能导致严重的疾病。 例如,已知阿尔茨海默病和肌萎缩侧索硬化症 (ALS) 等神经退行性疾病会伴随神经元中蛋白质的异常积聚。 然而,这种积累背后的触发因素仍然未知。 由东京都立大学安藤香苗副教授领导的一个研究小组一直试图通过研究果蝇来确定蛋白质异常积累的原因,果蝇是一种普遍研究的模式生物,与人类生理学有许多关键相似之处。 他们关注的是轴突中线粒体的存在,轴突是一种长卷须状的附属物,从神经元中伸出,形成必要的连接,使信号在我们的大脑内传输。 众所周知,轴突中的线粒体水平会随着年龄的增长以及神经退行性疾病的进展而下降。 现在,研究小组发现轴突中线粒体的消耗对蛋白质的积累有直接影响。 他们利用基因改造来抑制米尔顿的产生,米尔顿是线粒体沿轴突运输的关键蛋白质。 研究发现,这导致果蝇神经元中蛋白质含量异常,这是细胞自噬(细胞中蛋白质回收)崩溃的结果。 通过蛋白质组学分析,他们能够识别 eIF2β 的显着上调,eIF2β 是 eIF2 蛋白复合物的关键亚基,负责启动蛋白质产生(或翻译)。 eIF2α 亚基也被发现经过化学修饰。 这两个问题都阻碍了 eIF2 的健康发挥。 重要的是,通过人为抑制 eIF2β 的水平,研究小组发现他们可以恢复丢失的自噬,并恢复一些因轴突线粒体丢失而受损的神经元功能。 这不仅表明轴突中线粒体的消耗会导致蛋白质异常积累,而且这是通过 eIF2β 的上调而发生的。 随着人口老龄化和神经退行性疾病患病率的持续增加,该团队的研究结果为开发治疗这些严重疾病的疗法迈出了至关重要的一步。 资金: […]
中间神经元引导大脑发育过程中的神经转换
概括: 研究人员发现了特定中间神经元在大脑发育中的关键作用。 该研究确定了两种类型的中间神经元:SST+ 和 PV+,它们在出生后的早期阶段协调从同步到异步神经元活动的转变。 这种转变对于大脑有效处理感官信息的能力至关重要。 通过了解这些中间神经元如何调节大脑成熟,该研究揭示了各种神经发育障碍的潜在机制。 关键事实: 该研究确定 SST+ 中间神经元是同步神经模式的启动者,PV+ 中间神经元是发育中大脑向异步活动过渡的促进者。 SST+ 中间神经元也会影响 PV+ 中间神经元的成熟,突出了对大脑及时发育至关重要的分层相互作用。 这些发现对于理解与这些中间神经元相关的神经发育障碍具有重要意义,为研究它们在自闭症和精神分裂症等疾病中的作用提供了新的途径。 发育神经生物学中心和 MRC 神经发育障碍中心的科学家发表了一项研究 神经元 该研究确定了两种类型的中间神经元,即大脑的抑制性神经元,作为大脑关键发育过程的指导者。 在出生后的早期发育过程中,大脑网络的特点是同步大量神经元的爆发性活动。 随着大脑的成熟,这种活动模式的节奏、频率和幅度会发生变化,变得异步,只有一小部分神经元同时活动。 大脑皮层含有大量不同的中间神经元。 图片来源:神经科学新闻 这些变化使大脑能够处理和适应我们的感官接收到的大量信息。 尽管神经元活动模式之间的这种转变是大脑发育的一个重要里程碑,但这一过程背后的细胞机制仍然知之甚少。 在这项研究中,奥斯卡·马林领导的实验室试图调查这一转变背后的关键人物。 科学家们观察到,抑制信号的增加导致了这种转变。 虽然兴奋性和抑制性信号塑造了早期发育的大脑,但抑制性信号比兴奋性信号出现得晚。 中间神经元(产生这些抑制信号的细胞)的逐渐成熟决定了大脑功能的发展。 大脑皮层含有大量不同的中间神经元。 在这项研究中,他们确定了在小鼠出生后发育的前两周内负责调节网络活动的特定中间神经元。 SST+ 中间神经元产生神经元活动的同步模式,而 PV+ 中间神经元负责向异步活动模式的转变。 他们还发现 SST+ 中间神经元部分控制 PV+ 中间神经元的成熟,从而指导这种转变的时间。 此外,阻止 SST+ 中间神经元发挥作用会导致大脑发育延迟。 这些结果证实了 SST+ 中间神经元作为发育中大脑神经元动力学的关键调节因子的作用。 “我们已经确定了整合和调节大脑发育关键阶段的中间神经元的亚类。 这些中间神经元(SST+ 和 PV+ 中间神经元)也与多种神经发育状况有关。 “这些发现表明,我们需要进一步研究这些中间神经元,以更好地了解这些情况,”神经科学教授、本研究的资深作者、FMedSci […]
希腊和罗马时代痴呆症很罕见
概括: 严重的记忆丧失(类似于今天的痴呆症流行)在古希腊和罗马极为罕见,这表明这些情况可能很大程度上源于现代生活方式和环境。 通过分析古典文献,研究发现这些古代文明中很少提及认知障碍,这与当前的痴呆症发病率形成鲜明对比。 与过着前工业化生活方式且痴呆症发病率较低的提斯曼美洲印第安人相比,进一步支持了体力活动水平和环境因素显着影响痴呆症患病率的理论。 这一历史和比较分析强调了久坐行为和污染对认知健康的影响,为预防现代痴呆症提供了见解。 关键事实: 古希腊和罗马文献中很少有认知障碍的案例,这表明像阿尔茨海默病这样的疾病在 2000 年前是罕见的。 该研究将古代痴呆症患病率与提斯曼人的患病率进行了对比,提斯曼人由于积极的前工业化生活方式而痴呆症发病率较低。 空气污染和久坐行为等环境因素被认为是现代痴呆症病例增加的重要因素。 来源: 南加州大学 您可能认为与年龄相关的痴呆症一直伴随着我们,可以追溯到古代世界。 但对古典希腊和罗马医学文献的一项新分析表明,在 2000 至 2500 年前的亚里士多德、盖伦和老普林尼时代,严重的记忆丧失(在今天的流行水平上发生)极为罕见。 南加州大学领导的研究发表在 阿尔茨海默病杂志, 支持这样一种观点,即阿尔茨海默病和相关痴呆症是现代环境和生活方式的疾病,久坐行为和接触空气污染在很大程度上是罪魁祸首。 芬奇推测,随着罗马城市变得更加密集,污染加剧,导致认知能力下降的情况增多。 图片来源:神经科学新闻 “古希腊人非常非常少——但我们发现了他们——提到了类似轻度认知障碍的东西,”第一作者、南加州大学伦纳德·戴维斯老年学学院教授卡勒布·芬奇说。 “当我们到达罗马时,我们发现了至少四个陈述表明存在晚期痴呆症的罕见病例 – 我们无法判断它是否是阿尔茨海默氏症。 因此,从古希腊人到罗马人有一个进步。” 古希腊人认识到,衰老通常会带来记忆问题,我们将其称为轻度认知障碍(MCI),但远不及阿尔茨海默氏症和其他类型的痴呆症引起的记忆、言语和推理能力的严重丧失。 芬奇和合著者、洛杉矶加州州立大学历史学家斯坦利·伯斯坦(Stanley Burstein)仔细研究了希波克拉底及其追随者的大量古代医学著作。 该文本列出了老年人的疾病,如耳聋、头晕和消化系统疾病,但没有提及记忆丧失。 几个世纪后的古罗马,突然出现了一些提及。 盖伦指出,到了80岁,一些老年人开始难以学习新事物。 老普林尼指出,参议员和著名演说家瓦莱里乌斯·梅萨拉·科维努斯忘记了自己的名字。 西塞罗谨慎地指出,“老年人的愚蠢……是不负责任的老人的特征,但不是所有老人的特征。” 芬奇推测,随着罗马城市变得更加密集,污染加剧,导致认知能力下降的情况增多。 此外,罗马贵族使用铅炊具、铅水管,甚至在酒中添加醋酸铅来使其变甜——无意中让自己中毒了强大的神经毒素。 (一些古代作家认识到含铅材料的毒性,但直到进入 20 世纪才在处理这个问题上取得很少进展。一些学者将罗马帝国的衰落归咎于铅中毒。) 在这篇论文中,芬奇不仅仅考虑了罗马帝国或希腊人。 由于缺乏古希腊和罗马的人口数据,芬奇转向了一个令人惊讶的古代老龄化模型:今天的提斯曼美洲印第安人,玻利维亚亚马逊的土著人民。 提斯曼人——就像古希腊人和古罗马人一样——拥有非常活跃的前工业化生活方式,而且他们的痴呆症发病率极低。 由南加州大学伦纳德·戴维斯学院心理学、老年学和预防医学教授玛格丽特·盖茨领导的国际认知研究小组发现,在提斯曼老年人中,只有约 1% 患有痴呆症。 相比之下,据阿尔茨海默病协会称,美国 65 岁及以上的老年人中有 11% 患有痴呆症。 “提斯曼的数据相当深入,非常有价值,”芬奇说。 “这是记录最齐全的大量痴呆症程度最低的老年人口,所有这些都表明环境是痴呆症风险的一个巨大决定因素。 […]
音乐的治愈笔记:缓解压力的特朗普流派特征
概括: 音乐的具体特征,而不是流派,在压力恢复中发挥着至关重要的作用。 这项涉及 470 名参与者的研究发现,无论音乐风格如何,缓解压力的歌曲通常都有一些共同特征。 研究表明,与听随机音符的人相比,听具有某些特征的音乐的人从压力中恢复得更快。 这项研究强调了在音乐治疗中关注音频特征而不是流派的重要性。 关键事实: 缓解压力的歌曲通常分为两类:大调柔和的曲调或小调模式的充满活力的曲目。 研究中听具有这些特定特征的音乐的参与者表现出从压力中恢复得更快。 Adiasto 的研究强调了音乐在缓解压力方面的个人性质,并建议音乐研究人员需要关注音频特征而不是流派。 来源: 拉德堡德大学 感到压力大吗? “带我回家,乡间小路”、“一切都无关紧要”或“再宝贝一次”可能会让你再次平静下来。 心理学家和音乐科学家 Krisna Adiasto 发现,音乐流派似乎在我们选择缓解压力的歌曲中没有发挥作用,但有效的歌曲具有共同的特征。 Krisna Adiasto 将于 1 月 29 日从拉德堡德大学获得博士学位。 在一个持续的压力会导致心血管疾病、倦怠和抑郁的社会中,寻找有效的压力缓解方法非常重要。 除了冥想或跑步之外,许多人还听音乐来放松。 “研究表明,音乐与治疗相结合可以产生良好的效果,”心理学家克里斯娜·阿迪亚斯托说。 “但是关于听音乐本身,研究尚不清楚。 并不是每个人在听了几首歌后都会感觉好一些。” 音乐相似之处 阿迪亚斯托和同事研究了哪种音乐最能帮助缓解压力以及原因。 研究人员通过问卷调查向 470 名不同国籍的参与者询问了哪些歌曲可以帮助他们在压力过后感觉更好。 “我们得到的答案令人惊讶,”阿迪亚斯托说。 “看看过去的研究,你可能会认为大多数人会选择古典音乐,但选择的歌曲范围从硬派到古典,从配乐到氛围音乐。” 根据调查问卷编制了 1,296 首歌曲的列表。 研究人员发现,缓解压力的歌曲具有共同的特征。 Adiasto 和同事将它们分为两类:大调柔和的歌曲,如 Maroon 5 的《Memories》和 John Denver 的《Take Me Home, Country Roads》;以及小调调相当充满活力的歌曲,如《Shape》艾德·希兰的《of […]
自闭症的间接遗传影响被揭示
概括: 研究人员通过关注特殊基因突变及其对邻近基因的影响,在理解自闭症谱系障碍(ASD)的遗传学方面取得了重大突破。 研究表明,由于基因组的三维结构,某些基因组区域的启动子内的突变可以间接影响 ASD 相关基因。 这一发现挑战了传统上对蛋白质编码区和 ASD 相关基因直接突变的关注,为 ASD 复杂的遗传结构提供了新的见解。 关键事实: 该研究发现,特定拓扑关联域 (TAD) 内基因组启动子的从头突变可能会影响 ASD 相关基因。 研究人员使用了超过 5,000 个家庭的大型数据集,使这项研究成为最广泛的 ASD 全基因组研究之一。 这一发现对自闭症谱系障碍的未来诊断和治疗策略具有影响,表明需要超越直接基因突变的范围。 来源: 王国 RIKEN 脑科学中心 (CBS) 的研究人员通过分析个人及其家庭基因组的突变来研究自闭症谱系障碍 (ASD) 的遗传学。 他们发现,一种特殊的基因突变与典型突变的作用方式不同,它对这种疾病的影响如何。 本质上,由于基因组的三维结构,突变能够影响与自闭症谱系障碍相关的邻近基因,从而解释了为什么即使自闭症谱系障碍相关基因没有直接突变,自闭症谱系障碍也会发生。 这项研究发表在杂志上 细胞基因组学。 涉及更多家庭和患者的进一步研究对于更好地了解自闭症谱系障碍的遗传根源至关重要。 图片来源:神经科学新闻 自闭症谱系障碍(ASD)是一组以重复行为和社交互动困难为特征的疾病。 尽管它在家族中遗传,但其遗传力的遗传学很复杂,而且人们对它的了解还只是部分。 研究表明,高度的遗传力不能简单地通过观察基因组中编码蛋白质的部分来解释。 相反,答案可能在于基因组的非编码区域,特别是启动子,基因组中最终控制蛋白质是否实际产生的部分。 RIKEN CBS 的 Atsushi Takata 领导的研究小组检查了基因组这些部分中的“从头”基因变异(不是从父母遗传的新突变)。 研究人员分析了超过 5,000 个家庭的广泛数据集,使其成为迄今为止世界上最大的自闭症谱系障碍全基因组研究之一。 他们专注于 TAD——基因组中的三维结构,允许附近不同基因及其调控元件之间的相互作用。 他们发现,只有当启动子位于包含 ASD 相关基因的 TAD […]
