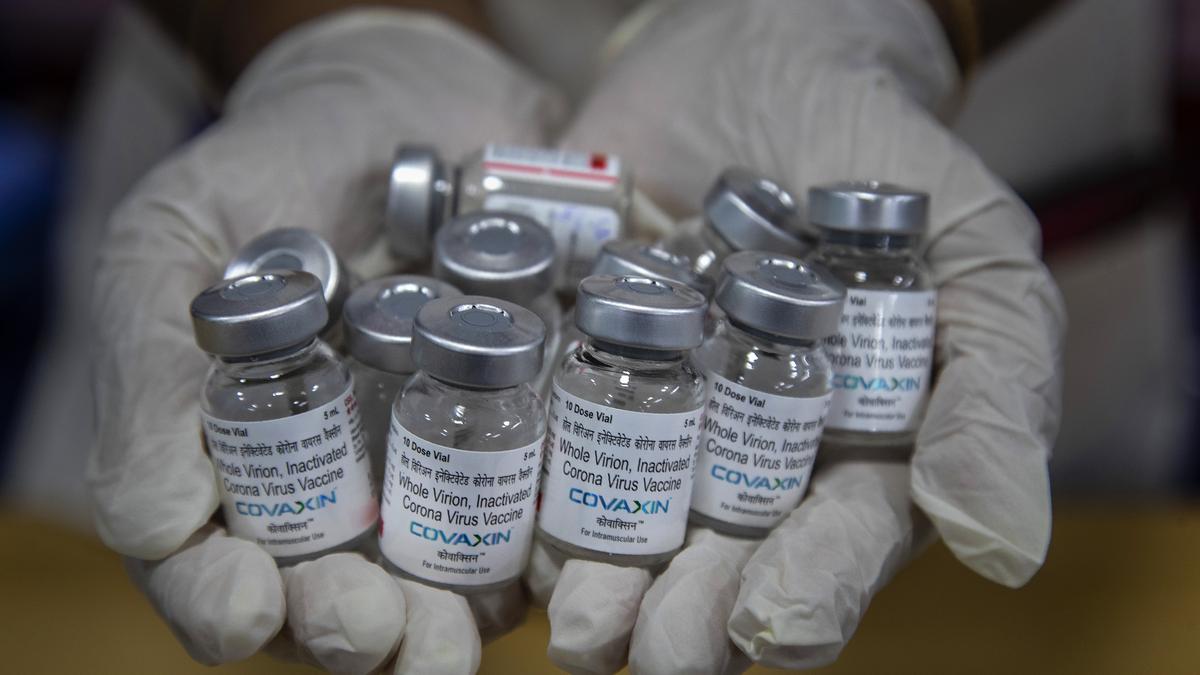
到目前为止的故事: 印度医学研究理事会(ICMR)发布 致贝拿勒斯印度教大学研究人员的一封信 上周,反驳 他们对印度本土 COVID 疫苗副作用的研究 — Covaxin。在研究论文发表在同行评议期刊几天后,ICMR 负责人 Rajiv Bahl 发出了反驳,声称他的机构在论文中被错误且误导性地承认。他指出了这项“设计不良的研究”中所谓的“严重缺陷”。值得注意的是,ICMR 与 Bharat Biotech 一起参与了 Covaxin 的开发。
BHU 的研究得出了什么结论?
研究表明,47.9% 的青少年和 42.6% 的成年人报告了病毒性上呼吸道感染。青少年中常见的 AESI 是新发皮肤和皮下疾病、全身疾病和神经系统疾病。成年人中常见的 AESI 是全身疾病、肌肉骨骼疾病和神经系统疾病。4.6% 的女性参与者出现月经异常。2.7% 和 0.6% 的参与者出现眼部异常和甲状腺功能减退。在严重 AESI(1%)中,0.3% 和 0.1% 的参与者被确诊为中风和格林-巴利综合征。
对此,与 ICMR 自己的国家病毒学研究所合作开发候选疫苗的疫苗制造商 Bharat Biotech 表示,为了使此类安全性研究有效且信息丰富,并避免研究人员的偏见,还需要一些数据点。 其中包括受试者在参与研究之前的 AESI 安全性概况;研究过程中未接种疫苗的受试者的安全性概况的比较;研究过程中接种其他疫苗的受试者的安全性概况的比较等。
ICMR 反对什么?
巴尔博士在信中表示,ICMR 与这项研究无关,也没有提供任何资金或技术支持。他声称,作者在没有事先批准或通知该机构的情况下承认 ICMR 为研究提供了支持,称这是“不恰当和不可接受的”。
关于研究本身,他声称存在严重缺陷:该研究没有未接种疫苗的对照组与接种疫苗的对照组进行比较,因此,研究中报告的事件无法与 COVID-19 疫苗接种联系起来或归因于疫苗接种;它没有提供在一般人群中观察到的模式的背景率,因此无法研究接种疫苗后观察到的事件。此外,Bahl 博士声称没有研究参与者的基线信息;研究工具与参考论文中定义的 AESI 不一致,数据收集方法也不一致(通过电话联系参与者,并在没有任何临床确认的情况下记录他们的回答)。

他进一步要求研究人员删除对 ICMR 的致谢并发布勘误表。他的信中还要求撤回该论文,并附上注释:“这篇论文隐含地得出了没有证据支持的疫苗安全性结论。” BHU 记录显示,它已收到发给其研究人员的通报。研究人员已将他们的回应传达给 ICMR。
后果是什么?
大多数研究人员对 ICMR 的回应感到震惊,称其为“学术审查”。社交媒体上的多名医生和研究人员账户也指出,ICMR 与该公司共同开发了疫苗,没有声明其既得利益也是研究方面的严重失误。在做出官方回应的组织中,首当其冲的是一群研究人员、医生和公共卫生专家组成的“全民健康组织”(UHO),他们与研究生态系统一样对这一迟来的否认感到震惊。UHO 给 ICMR 写了一封公开信,称这项研究填补了实地数据分析方面的关键空白,分析了 Covaxin 的安全性。
“虽然我们希望并期待 ICMR 能在此研究的基础上继续研究,解决其不足之处,并提高疫苗安全标准,但我们惊讶地发现 ICMR 发来要求撤回该论文并威胁研究作者的信件,”信中写道。信中说,关于没有对照组,这确实是一个缺点,但研究本身已经承认了这一点。此外,这实际上表明 ICMR 有权访问对照组的数据——Covaxin 的原始 3 期试验。它指控 ICMR 和该公司都没有发表长期安全试验。虽然使用电话采访并不理想,但 ICMR 过去曾使用过这种方式,甚至在关于 COVID 疫苗的论文中也是如此。信中补充说,以这样的方式要求撤回 BHU 的论文,与 ICMR 这样地位的科学机构不相称。
1716703423
2024-05-25 21:51:00




:quality(70)/cloudfront-eu-central-1.images.arcpublishing.com/liberation/FYLCQT5Z65BO3OXMOGD2HKGYVY.jpg)







