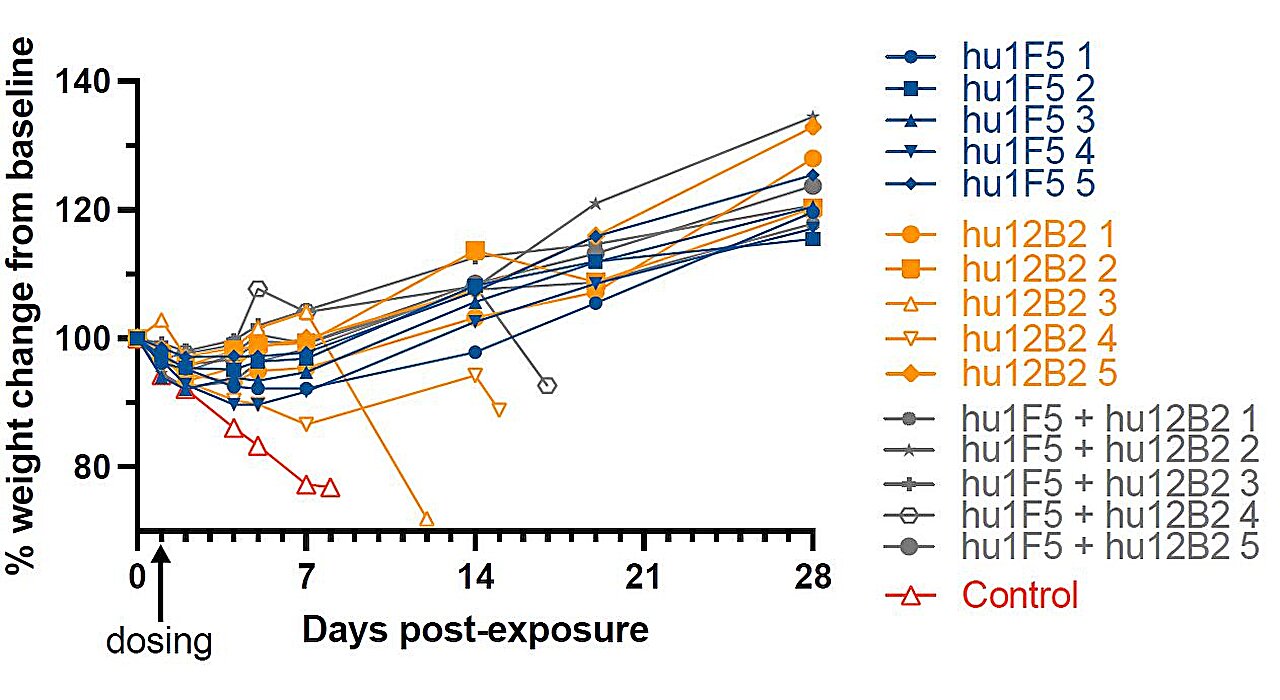
图表显示,使用 hu1F5、hu12B2 或两种抗体治疗的尼帕病毒病小鼠体重相对于基线的百分比变化。空心符号表示死于疾病的仓鼠。来源:Zeitlin 等人,Sci. Transl. Med. 16,eadl2055 (2024)
一种实验性单克隆抗体已被设计用于对抗致命的尼帕病毒,这是一种新出现的人畜共患病原体,人类死亡率高达惊人的 90%。
这种候选单克隆抗体是由圣地亚哥一家生物制药公司与多家研究最致命新兴病毒的美国学术中心联合研发的。针对多种人畜共患病毒的治疗方法的研发迫在眉睫。新兴病原体有可能引发流行病,或落入可能利用它们进行生物恐怖主义的恶意势力之手。
圣地亚哥 Mapp Biopharmaceutical 公司联合创始人、新研究的主要作者 Larry Zeitlin 博士写道:“目前还没有针对尼帕病毒感染者的获批疫苗或疗法。” 已报告 在科学转化医学杂志上发表的文章“尼帕病毒是一种高致病性人畜共患副粘液病毒,在南亚和东南亚地区经常引起人类和动物的暴发。”
和埃博拉病毒、SARS、SARS-CoV-2 和马尔堡病毒一样,尼帕病毒病原体也起源于蝙蝠。尼帕病毒的名称源自 1990 年代末马来西亚一个养猪户感染该病毒的村庄的名称。麻疹病毒虽然不是源自蝙蝠,但它是副粘液病毒家族的另一个成员,是科学界已知的最具传染性的病毒之一。虽然尼帕病毒的传染性不如麻疹,但其死亡率却要高得多。
感染尼帕病毒的人可能会出现危险的呼吸障碍和脑肿胀,这些症状会导致死亡率极高。死亡率从 40% 到 90% 不等。该病毒是孟加拉国和印度最近爆发多起疫情的罪魁祸首。
在开展这项新研究之前,Zeitlin 及其同事已经开发出一种单克隆抗体,他们将其命名为 m102.4。它具有中和尼帕病毒的能力,有时会根据同情用药方案给患者使用。现在,Zeitlin 和他的合作者开发出了一种改进的单克隆抗体,名为 hu1F5,它针对的是尼帕病毒 F 蛋白的融合前形式。科学家已经在动物模型中测试了这种新的单克隆抗体。
Zeitlin 在报告中指出:“我们假设,针对 F 糖蛋白融合前构象的 mAb(单克隆抗体)可能比 m102.4 提供更好的保护。”“为了验证这一点,我们在仓鼠模型中比较了两种针对尼帕病毒 F 蛋白的强效中和 mAb,hu1F5 和 hu12B2。Hu1F5 提供的保护优于 hu12B2,因此被选中与 m102 进行比较。”
在仓鼠中,研究小组发现,感染仓鼠一天后注射 hu1F5 可使 100% 的仓鼠存活。值得注意的是,即使在感染五天后注射,hu1F5 也能保护非洲绿猴免受尼帕病毒的感染。在该研究中,所有六只受感染的动物都存活了下来。Hu1F5 的表现也优于早期的单克隆抗体 m102.4,后者只能保护六只接受治疗的动物中的一只免于死亡。
研究团队还在抗体中引入了几处突变以延长其半衰期,并报告说,在动物试验中表现优异的单克隆抗体正在进入第一阶段人体临床试验。
Mapp Biopharmaceutical 由 Zeitlin 和 Kevin Whaley 博士于 2003 年创立。他们的目标是开发用于预防和治疗传染病的新型药物,重点关注全球健康和生物防御。
5 月,该公司宣布与美国卫生与公众服务部下属的生物医学高级研究与发展局(BARDA)合作。该研究重点是针对马尔堡病毒的单克隆抗体。
在当前涉及抗尼帕病毒单克隆抗体的研究中,泽特林和 Mapp Biopharmaceutical 的同事与来自美国各地的科学家合作。合作者包括德克萨斯大学医学分校、加尔维斯顿国家实验室的团队;田纳西州纳什维尔范德堡大学医学中心病理学、微生物学和免疫学系;西雅图华盛顿大学生物化学系,以及马里兰州贝塞斯达军校微生物学和免疫学系的一个团队。
同时,Zeitlin 和多中心团队得出结论,针对尼帕病毒融合糖蛋白的交叉反应单克隆抗体的治疗给药可保护非人类灵长类动物。动物模型研究的结果支持进一步开发 hu1F5 用于人类尼帕病毒感染。
更多信息:
Larry Zeitlin 等人,针对尼帕病毒融合糖蛋白的交叉反应 mAb 的治疗性给药可保护非人类灵长类动物,科学转化医学 (2024)。 DOI: 10.1126/scitranslmed.adl2055
© 2024 科学X网络
引用:科学家正在开发一种单克隆抗体来中和最致命的人畜共患病原体之一尼帕病毒(2024 年 6 月 29 日)于 2024 年 6 月 29 日检索自
本文件受版权保护。除出于私人学习或研究目的的合理使用外,未经书面许可不得复制任何部分。内容仅供参考。
2024-06-29 13:50:01
1719670529
#科学家正在开发一种单克隆抗体来中和最致命的人畜共患病原体之一尼帕病毒